Российские ученые создали простой и высокоэффективный способ нейтрализации фосфорорганических соединений — основы большой части боевых отравляющих веществ. Противоядие с помощью нанотранспортера удается доставить непосредственно к месту действия яда и химически блокировать его.

Ввиду огромных запасов фосфорорганических отравляющих веществ новые средства химической защиты никогда не будут лишними
Фото: AP
Начало этой истории нужно отнести к 1938 году, когда два немецких химика из крупного концерна IG Farben пытались получить эффективный пестицид, но создали боевое отравляющее фосфорорганическое вещество зарин. Оно и поныне часто используется террористами — достаточно вспомнить трагические события в токийском метро. Формула была немедленно передана в вермахт, и появились еще три печально известных вещества G-серии: зоман, циклозарин и табун.
Так появились первые фосфорорганические боевые отравляющие вещества. Уже после войны в Британии и СССР были созданы самые совершенные убийцы той же группы — нервно-паралитические газы VX и VR. Совсем недавно название VX снова всплыло на лентах новостей: именно им был отравлен брат Ким Чен Ына, Кин Ен Нам. Впрочем, пестициды на основе фосфорорганики тоже делали и делают — и они тоже представляют собой большую опасность.
Как же действуют эти вещества?
Здесь нужно немного рассказать, как передается сигнал от нейрона к нейрону. В месте соединения двух нейронов существует так называемый синапс, электрический сигнал через который передается химическим путем: нейрон-передатчик выпускает в синаптическую щель нейромедиаторы (например, всем известные дофамин или серотонин), они связываются с рецепторами на нейроне-приемнике — и сигнал бежит дальше. В двигательных нервах таким нейромедиатором является ацетилхолин. Избыток ацетилхолина гидролизуется ферментом ацетилхолинэстеразой — нельзя, чтобы нервный импульс шел бесконечно.
Вот на этот-то фермент и действуют фосфорорганические отравляющие вещества. Они блокируют работу ацетилхолинэстеразы, что приводит к параличу.
Антидоты к ним начали разрабатывать давно. И успехи были, но, к сожалению, эти противоядия не гарантировали стопроцентный результат и требовали высокой дозы.
Ученые из МГУ под руководством энзимолога Елены Ефременко получили фермент органофосфатогидролазу, который очень эффективно блокирует действие нервно-паралитических ядов, но у него есть два серьезных недостатка. Первый из них связан с тем, что эта гидролаза — бактериальный фермент и воспринимается иммунной системой как чужеродное вещество, вызывая иммунный ответ, ослабляющий действие антидота. Более того, она сама по себе быстро выводится из организма. Второй --сама по себе органофосфатогидролаза не очень стабильна и способна разложиться всего за месяц при нулевой температуре.
И здесь на помощь пришла еще одна разработка российского ученого, химика из МГУ, уехавшего работать в Университет Северной Каролины и Университет Небраски, Александра Кабанова.
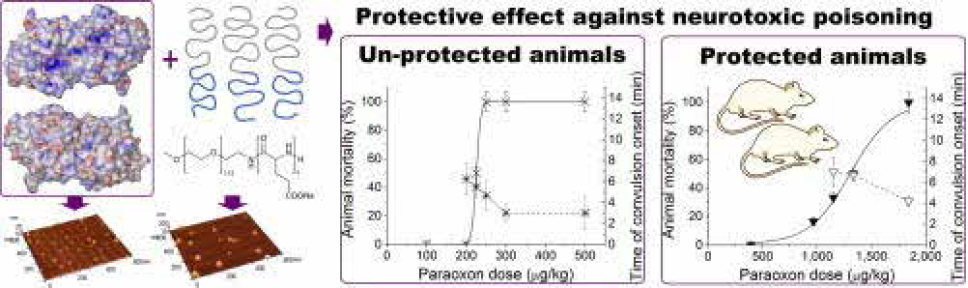

Объединение фермента-противоядия с полимером (левая часть рисунка) кардинально повышает выживаемость в контрольной группе мышей, получивших смертельную дозу фосфорорганического яда
Объединение фермента-противоядия с полимером (левая часть рисунка) кардинально повышает выживаемость в контрольной группе мышей, получивших смертельную дозу фосфорорганического яда
В 2010 году он совместно с профессором МГУ Натальей Клячко получил мегагрант и создал лабораторию по улучшению уже разработанных им так называемых нанозимов — наноразмерных полимерных мицелл, "транспортных емкостей" для доставки ферментов (энзимов) в мозг для лечения инсультов, болезни Паркинсона и других болезней.
"В 1980-х годах наша группа в Москве и независимо японские коллеги под руководством профессора Казунори Накаоки начали использовать полимерные мицеллы для доставки малых молекул в качестве лекарств. С тех пор область наномедицины переживает взрывной рост — сейчас такие наноразмерные агенты создают в сотнях лабораториях по всему миру",— комментирует Александр Кабанов.
Оказалось, что такие нанозимы, получающиеся самосборкой под действием электростатического взаимодействия фермента и полимера — идеальная оболочка для органофосфатогидролазы. Нанозимы позволяют транспортировать фермент к месту действия яда, "обманывая" иммунную систему. Кроме того, как оказалось, сама по себе нанозимная оболочка намного увеличивает срок хранения антидота — новый "упакованный" фермент прекрасно живет до трех лет.
Эксперименты уже подтвердили эффективность противоядия. Конечно же, на мышах. Животным вводили смертельную дозу VX или пестицида пароксона, а перед тем или сразу после вводили антидот. Выжили все животные, которым ввели пестицид, и 80% отравленных VX. В контрольной группе, разумеется, все животные погибли.
Оригинальное исследование опубликовано в Journal of Controlled Release под названием "Простой и высокоэффективный каталитический нанозимный нейтрализатор фосфорорганических нейротоксинов".
Как говорят ученые, новый препарат мог бы спасти Ким Ен Нама — в случае немедленного введения после отравления. Что гораздо более важно, он может спасти сотни тысяч людей, которые ежегодно умирают в мире от отравления пестицидами: нанозимы с ферментом лучше всего действуют после превентивного введения. А значит, их можно применять в качестве профилактического средства химической защиты.



