С помощью методов генной инженерии удалось модифицировать систему редактирования ядерной ДНК генома животных. Теперь она способна проходить в митохондрии и исправлять мутации в митохондриальной ДНК, связанные с до сих пор не излечимыми наследственными болезнями.
В 1871 году немецкий врач Теодор Лебер публикует работу, в которой описывает 15 случаев наследственной атрофии зрительных нервов в четырех семьях. Прошло больше ста лет, прежде чем в 1988 году американский биохимик Дуглас Уоллес обнаружил мутацию в митохондриальной ДНК (мтДНК), связанную с заболеванием, описанным Лебером.
Наследственная атрофия зрительных нервов Лебера (LHON) — наиболее распространенное заболевание, вызванное мутациями в мтДНК; им страдает один человек на каждые 45 тысяч. Клинически заболевание проявляется как безболезненная потеря зрения обоих глаз и, к сожалению, до сих пор не лечится.

Что такое митохондрии
В нескольких научных лабораториях в разных странах разрабатываются методы генной терапии заболеваний, обусловленных мутациями в ДНК митохондрий. Однако подавляющее большинство таких исследований основаны на внесении в митохондрии дополнительного генетического материала или правильно функционирующего белка, которые компенсируют работу мутантной мтДНК. Основным минусом таких исследований является непродолжительность действия внесенного генетического материала или белка.
Новейшая система редактирования генома CRISPR/Cas9 была опубликована в 2012 году и буквально перевернула биоинженерию и биотехнологию. Благодаря этой системе у исследователей появилась возможность исправлять мутации в ДНК. С ее помощью можно вырезать фрагменты ДНК определенной длины и вставлять в выбранный исследователем локус ДНК нужные фрагменты.
Но хотя система CRISPR/Cas9 уже используется для редактирования ядерной ДНК, пока она не адаптирована для работы с ДНК митохондрий. Основная проблема заключается в доставке внутрь митохондрии составных элементов CRISPR\Cas9, а именно нуклеазы Cas9 и направляющей РНК, которая узнает мутацию.
Рис. 01 Система целенаправленного редактирования мтДНК
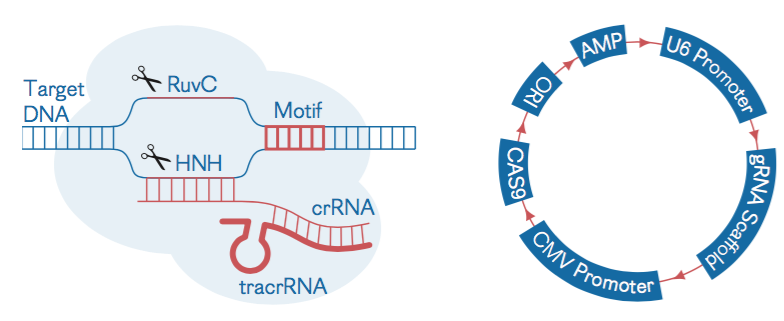
Рис. 02 Генетическая конструкция
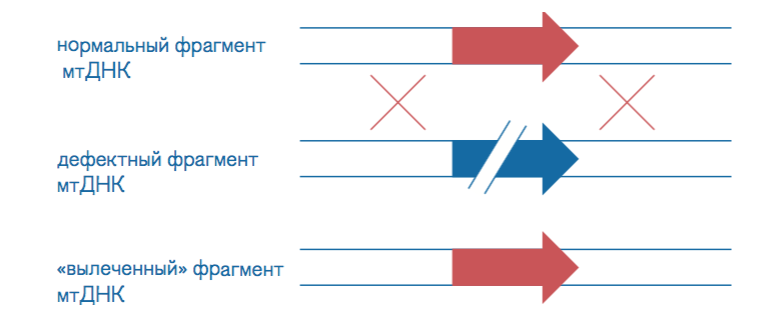
В нашем институте в тесном сотрудничестве с новосибирским Институтом цитологии и генетики при финансовой поддержке Министерства образования и науки РФ в рамках соглашения №14.575.21.0108 от 27.11.2014 (Уникальный идентификатор проекта: RFMEFI57514X0108), ведутся исследования по модификации генетической конструкции, кодирующей систему CRISPR/Cas9 рис. 01-02. В настоящее время эксперименты проводятся на цитоплазматических гибридных клеточных линиях (цибриды), которые представляют собой клетки пациента с мутантной митохондриальной ДНК, слитые с клетками остеосаркомы. Цибриды — удобная модель, они могут поддерживаться на питательной среде сколь угодно долго.
При успешном завершении экспериментов на клеточной линии они будут продолжены на модельных объектах — мышах. Детали экспериментов пока не разглашаются, поскольку находятся на стадии публикации и имеют стратегическое значение в области нейротехнологий. После завершения второго этапа тестирования системы CRISRP/Cas9 на животных начнутся клинические испытания. Есть все основания надеяться, что модифицированная система редактирования митохондриальной ДНК станет поворотной точкой в лечении многих нейромышечных и нейродегенеративных патологий.

