Как работают новые иммунотерапевтические противоопухолевые препараты направленного действия
Онкология
Министр здравоохранения Вероника Скворцова сообщила, что в России разработан противоопухолевый препарат, который показал фантастический результат по устранению метастазирующих меланом. Компания Biocad, создатель препарата, объяснила, что препарат блокирует антиген PD-1 (Programmed cell death 1) с помощью моноклонального антитела, и организм начинает распознавать и уничтожать раковые клетки. Осенью 2016 года начались клинические испытания препарата.
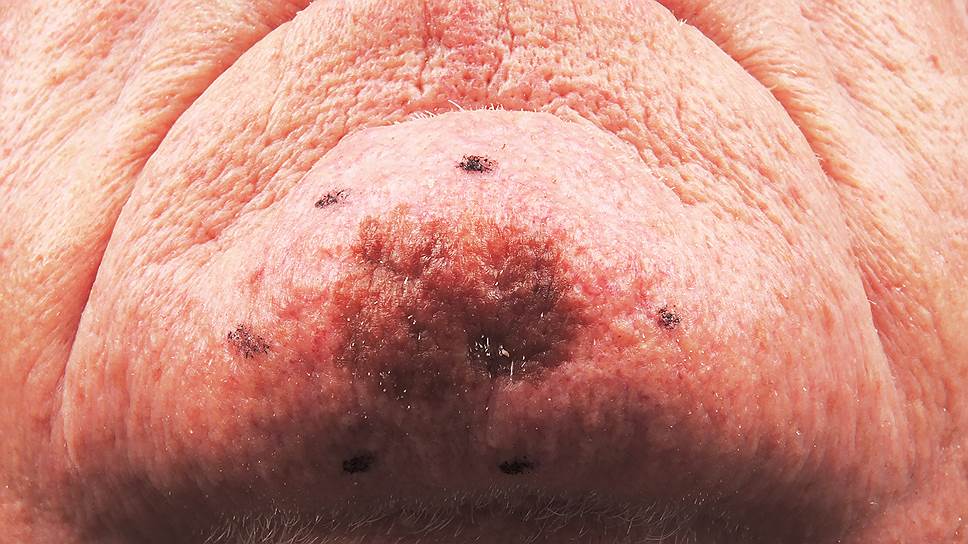
Отечественный препарат, который позволит повысить выживаемость пациентов при меланоме и некоторых других видах рака, должен появиться на рынке в 2018-2019 годах
Фото: AFP
Объявление о прорыве
Онкологические заболевания являются серьезной проблемой, решения которой еще не найдено. Несмотря на высокий уровень развития хирургии, химиотерапии, лучевой и таргетной терапии, высокая смертность пациентов требует поиска новых методов и путей борьбы с этой группой заболеваний.
Основным барьером на пути спонтанного образования опухолей в организме человека являются механизмы апоптоза и иммунная система. Апоптоз — запрограммированная гибель клетки, первое препятствие на пути развития опухоли. Клетка может подчиниться сигналу на самоуничтожение, который получает, если начинается аномальное развитие. К сожалению, из-за мутаций этот механизм иногда не срабатывает, тогда в действие вступает иммунная система, клетки которой в большинстве случаев способны обнаружить и уничтожить опухолевые клетки до начала патологического процесса. Если же опухоль вышла из-под иммунной регуляции, начался рак, организму требуется помощь.
В 2013 году журнал Science, а в 2015 году Американское общество клинической онкологии признали иммунотерапию рака прорывом года и главным достижением в области онкологии.
Что же произошло тогда, почему это было прорывом? Ответ прост: фармацевтические компании наконец, спустя 15 лет после первых сообщений ученых о механизме подавления раковыми клетками иммунного ответа организма, поверили в перспективность иммунотерапии, и на фармацевтический рынок вышли лекарственные препараты нового типа, позволившие изменить прогноз для многих онкологических больных. К сожалению, далеко не для всех, но ввиду того, что существующие методы во многом себя исчерпали, именно иммунотерапия дает надежду на дальнейший прогресс в борьбе с раком.
Что же такое иммунотерапия и что необычного в новых препаратах?

Этапы большого пути
Понимание того, как функционирует иммунная система организма, приходило постепенно. Первые успешные опыты по стимулированию иммунитета к борьбе с опухолью относятся к XIX веку: американский хирург Вильям Коли, заражая пациентов бактерией — возбудителем скарлатины, добился в ряде случаев регресса опухолей и даже, возможно, излечения больных. Но механизмы этого явления были непонятны, а альтернативные методы лечения выглядели эффективнее, и открытие доктора Коли оказалось не востребовано.
Еще одной попыткой применить неспецифичный стимулятор иммунитета в борьбе с опухолями стало использование противотуберкулезной вакцины — бациллы Кальметта--Геррена. Предложенная еще в 1929 году, эта методика была одобрена Агентством по безопасности пищевой продукции и лекарственных средств США (FDA) для лечения рака мочевого пузыря только в 1990 году.
Другой важной вехой в развитии представлений об иммунной системе стало открытие иммуноцитокинов — биологически активных белков, участвующих в регуляции иммунной системы. Ныне белки этого класса интерферон-альфа и интерлейкин-2 являются одними из самых эффективных противораковых препаратов, но их применение ограничено выраженной токсичностью такого лечения. Группа других цитокинов, объединенная под названием "фактор некроза опухолей", также нашла свое применение в борьбе с опухолями: они разрушают сети питающих растущую опухоль кровеносных сосудов.
Следующим этапом на пути к успеху иммунотерапии стало применение антител, которые позволяли затормозить развитие поверхностных антигенов опухоли, доставляя прямо в опухоль ("мишень", англ. target) токсичные или радиоактивные молекулы, смертоносные для клеток. Такие способы доставки лекарства строго по адресу называются "таргетной терапией" и уже прочно вошли в медицинскую практику.
Тут же следует упомянуть технологию модификации собственной иммунной системы человека путем замены или внесения дополнительного рецептора на поверхность Т-лимфоцитов, что позволяет перепрограммировать эти клетки и заставить узнавать нужный антиген.
Как разрушить «иммунитет» раковых клеток
Все эти этапы развития иммунологии и ее применения в онкологии сделали практически неизбежным следующий шаг. Рано или поздно исследователи должны были обнаружить механизм подавления иммунной системы со стороны опухоли, понять, как именно подавляется активность клеток иммунной системы, призванных уничтожать опухолевые клетки.
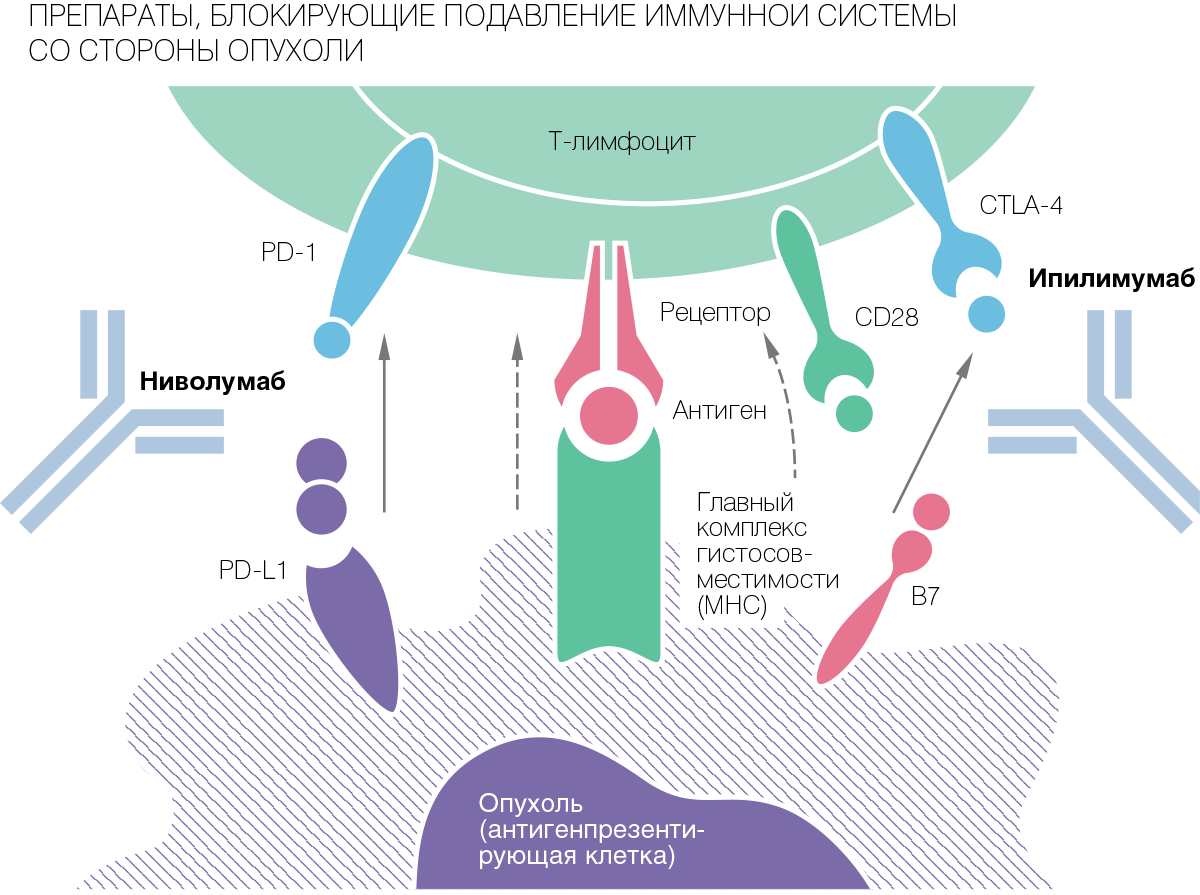
На сегодня известны два рецептора, CTLA-4 и PD-1, активация которых приводит к подавлению и даже уничтожению клеток иммунной системы, пытающихся начать бороться с опухолью. В норме эти рецепторы на поверхности антиген-презентующих клеток позволяют защитить собственные клетки организма от аутоиммунных реакций. Без них организм не смог бы выбраковывать и уничтожать опасные иммунные клетки, которые возникают в организме в виде неизбежной примеси к "нормальным" иммунным клеткам. Но как раз этот механизм опухолевые клетки используют для подавления реакций иммунной системы. Они экспрессируют? этот рецептор, что приводит к самоуничтожению (апоптозу) нормальных клеток иммунной системы, которые начинают реагировать на опухоль.
Первый современный иммунотерапевтический препарат ипилимумаб, который является моноклональным антителом, способным связывать и подавлять активность белка CTLA-4, позволил значительно улучшить результаты лечения больных метастатической меланомой.
Применение препаратов, подавляющих активность сигнального пути PD-1, позволило добиться еще более впечатляющих результатов в лечении метастатической меланомы. В исследовании на 418 пациентах показатель выживаемости в течение одного года составил 72,9% в группе, где больные принимали препарат ниволумаб, по сравнению с 42,1% при классической терапии.
Российские биотехнологические компании также включились в работу по разработке современных иммунотерапевтических препаратов. В 2018-2019 году на рынке должен появиться отечественный препарат, препятствующий связыванию рецептора Т-лимфоцитов PD-1 мишенью на поверхности опухолевой клетки, что позволит, по ожиданиям исследователей, повысить выживаемость пациентов при меланоме и некоторых других видах рака, использующих этот путь подавления иммунитета. Именно об этом препарате сообщила в конце прошлого года глава Минздрава РФ Вероника Скворцова (см. "Коммерсантъ" от 9 января 2017 года).
Открытие биологического процесса само по себе не приводит к победе над заболеванием
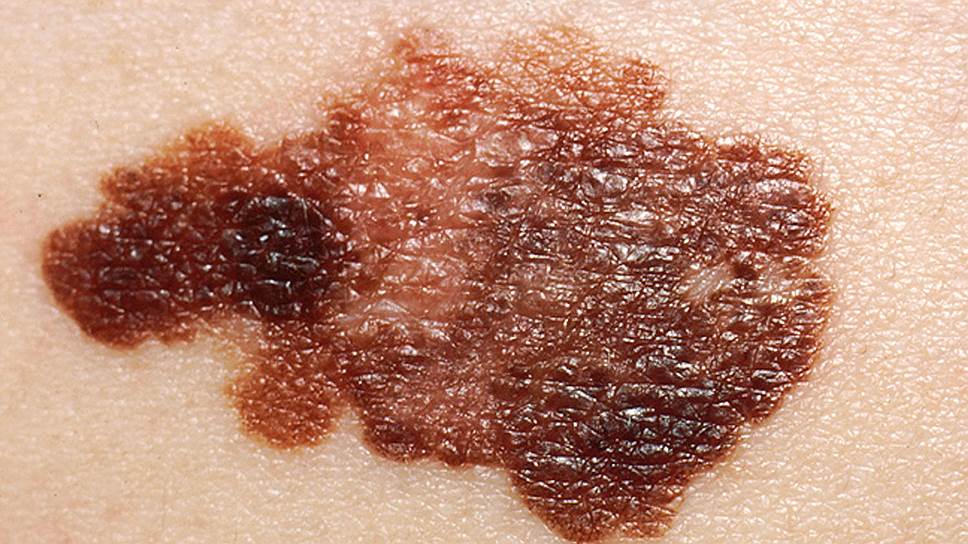
Иммунотерапевтические препараты могут сильно продлить жизнь больных меланомой
Фото: AFP
Шанс не для всех
Применение современных иммунотерапевтических препаратов позволяет добиться стойкого клинического ответа у части пациентов с различными злокачественными новообразованиями. Правда, несмотря на впечатляющие результаты, у большинства пациентов отмечается нечувствительность опухолей к препаратам этого класса и дальнейшее прогрессирование опухолевого процесса на фоне проводимого лечения.
Но главное, что отмечают исследователи, это не эффективность отдельных препаратов, которая оказалась в целом невысокой и проявлялась не во всех видах рака, а то, что открыт новый путь для борьбы с онкологическими заболеваниями посредством блокирования сигнального пути, который позволяет злокачественным клеткам уходить из-под надзора со стороны иммунной системы.
Таким образом, принципиально важным в развитии этого направления лекарственной терапии является поиск прогностических и предиктивных маркеров эффективности иммунотерапии, которые позволяли бы идентифицировать больных с иммуночувствительными опухолями.
Рисковать лучше деньгами, а не жизнями
Методы молекулярной и клеточной биологии дают широчайший набор инструментов для создания, проверки и производства биопрепаратов. Технология рекомбинантных белков позволяет в больших количествах нарабатывать биологически активные белки — основной элемент функционирования живых систем. Развитие технологии антител, открытие и широкое использование необычных нано-антител верблюда (см. "Наука", 2016, N2), создание антител с двойной специфичностью и способных мультимеризоваться, разработка технологии экономичного производства таких антител в животных-биореакторах — все это требует лишь указать цель, которая может быть эффективной точкой приложения накопленных сил для победы над раком.
Но открытие биологического процесса само по себе не приводит к победе над заболеванием. Ключевую роль играют производители лекарственных средств и государственные регуляторы. Для появления на рынке нового препарата требуются масштабные испытания, в том числе и на пациентах. Эффективность и безопасность зачастую обратно пропорциональны, а все проекты по разработке новых лекарств сопряжены с большими рисками. В этих условиях государство должно определять приоритеты и поддерживать исследования в высоко рискованных областях. Без динамичного развития научных исследований, без реализации прорывных проектов мы рискуем оказаться заложниками безопасных, но бесполезных лекарственных средств. Особенно обидно это будет сейчас, когда накопленный объем знаний о функционировании иммунной системы и открытие основных механизмов ее стимуляции и подавления позволяют рассчитывать на качественный прорыв в медицине в ближайшие годы и перейти на новый уровень борьбы с раком.
Эффективность и безопасность зачастую обратно пропорциональны, а все проекты по разработке новых лекарств сопряжены с большими рисками

