
Заражение
Африканская чума свиней (АЧС) — вирусная, контагиозная, септическая болезнь свиней, характеризующаяся лихорадкой, признаками токсикоза, геморрагическим диатезом и высокой летальностью. При острой, наиболее распространенной форме инфекции, 100% животных погибают в течение 5-10 суток. Поскольку вакцины против АЧС не разработаны, то для ликвидации и предупреждения распространения болезни во всем мире применяются стемпинг аут и жесткие карантинные мероприятия.
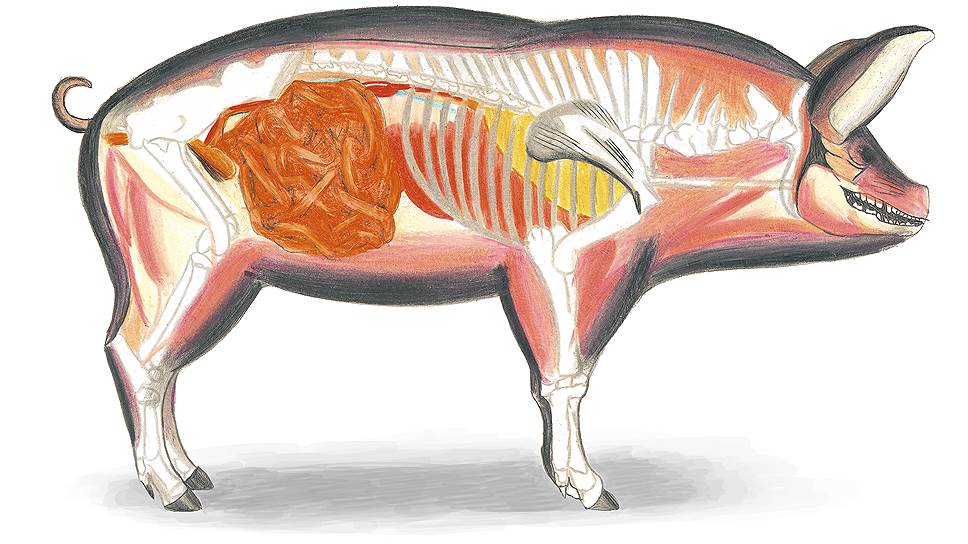
Патологоанатомические изменения при АЧС
Предыстория
На рубеже 60-х годов прошлого столетия, когда в мире были разработаны вакцины против полиомиелита, бешенства, кори, перспективы создания вакцин против вирусных болезней человека и животных представлялись весьма радужными. Поэтому, когда в 1957 и 1960 гг. АЧС впервые была занесена из Африки на Пиренейский полуостров, специалисты Португалии и Испании, получив аттенуированные, т.е. ослабленные в лабораторных условиях, штаммы, с согласия правительств вакцинировали около 600 тыс. свиней. Через несколько месяцев количество неблагополучных пунктов в обеих странах увеличилось в три-шесть раз, погибло до 50% привитого поголовья, у выживших свиней отмечали проявление клинических признаков болезни в поствакцинальный и отдаленный периоды. Негативные результаты широкомасштабного применения живых вакцин и последующие лабораторные исследования привели к формированию устойчивой позиции, что средства специфической профилактики АЧС на основе аттенуированных штаммов разработать невозможно, а ликвидацию болезни следует проводить посредством строгих ветеринарно-санитарных мероприятий, включающих тотальный убой свиней в очаге и угрожаемой зоне.

Опасен ли АЧС для людей
Первые попытки разработать вакцину
В 1960-х годах в связи с опасностью непреднамеренного или преднамеренного заноса вируса АЧС на территорию бывшего СССР было принято решение создать средства для временной защиты от болезни, чтобы обеспечить, как минимум, плановый убой свиней и переработку мясной продукции в комплексах, где содержали до 120-240 тыс. голов свиней. Специально для этого в г. Покров Владимирской области был построен ВНИИ ветеринарной вирусологии и микробиологии (сейчас — ГНУ ВНИИВВиМ Россельхозакадемии); институтским ученым помогли создать и научно-исследовательскую лабораторию в Народной республике Конго. Руководил проектом по "африканке" профессор Никифор Иванович Митин.
Параллельно с исследованиями по созданию средств специфической защиты от болезни накапливались данные о сероиммунотиповом плюралитете вируса АЧС. Первыми эту тему подняли британские и испанские ученые, но затем их интерес к этому направлению угас, а вот наши ученые по результатам реакции задержки гемадсорбции в культуре клеток и иммунологической пробы на свиньях создали сероиммунотиповую классификацию. Более ста хранившихся в институте изолятов и штаммов вируса АЧС со всего мира были разделены на девять сероиммунотипов. Для каждого из них надо было разрабатывать свои средства для временной защиты свиней.
.jpg)
Экономический ущерб от АЧС
В результате многократного пассирования, применения классических и весьма экзотических методов селекции в первичных и перевиваемых культурах клеток были получены аттенуированные штаммы (т.н. вакцинные) первых пяти сероиммунотипов. Они были безвредны для свиней в десятикратной прививочной дозе и на 14-е сутки обеспечивали формирование защиты продолжительностью не менее 4 месяцев. Все вакцинные штаммы соответствовали и другим требованиям: не передавались контактно при совместном содержании с интактными животным, не ревертировали в пяти последовательных пассажах на свиньях, были слабореактогенными. В зависимости от способов и целей применения были разработаны различные формы экспериментальных вакцин: нативные, концентрированные, лиофилизированные и эмульгированные. Предполагалось, что применять вакцины против АЧС в промышленных свинокомплексах закрытого типа можно будет только по специальному разрешению Главного управления ветеринарии МСХ СССР. Однако крупномасштабные эксперименты и лабораторные исследования с иммунологически ослабленными животными, включая супоросных свиноматок, подтвердили вероятность повторения негативного опыта испанских и португальских ученых. В результате сочли, что разработанные живые вакцины вряд ли будут когда-либо востребованы.

АЧС в России
Современное состояние исследований
Неудачи в создании живых, инактивированных, субъединичных вакцин стимулировали исследования свойств вируса, иммунологических механизмов защиты при АЧС, поиск протективных белков.
Профессор В.В. Макаров на основании обобщения полученных во ВНИИВВиМ экспериментальных данных сформулировал иммунологическую концепцию, согласно которой: 1) нейтрализация вируса АЧС антителами невозможна ввиду того, что вирус проникает в клетки-мишени (моноциты, макрофаги) путем фагоцитоза независимо от специфических рецепторов, а образование комплекса "вирион + антитело", наоборот, усиливает фагоцитоз по типу опсонизации; 2) ограничение репродукции вируса АЧС в организме свиньи происходит посредством противоклеточных эффекторных механизмов иммунитета, при этом критическую протективную роль выполняют цитотоксические Т-лимфоциты, которые, как правило, не индуцируются инактивированными и субъединичными вакцинами. Доказано, что важен и антителозависимый цитолиз нормальными киллерами.
Исходя из локализации в оболочке вирионов и плазматической мембране зараженных клеток, из сотни вирусных белков определены четыре-пять потенциально протективных. По логике, решающую роль в индукции защиты при АЧС должен играть белок, обладающий свойством серотиповой специфичности, который феноменологически обнаруживает себя в реакции задержки гемадсорбции. В 1990-х годах нами был идентифицирован серотипоспецифический гликопротеин, а испанскими исследователями — ген, кодирующий синтез вирусного CD-подобного белка, который отвечает за гемадсорбцию. Так разными путями был найден один и тот же критически важный для формирования противовирусной защиты белок.
В ведущих вирусологических центрах мира сейчас исследуют защитные свойства рекомбинантных конструкций, кодирующих синтез потенциально протективных белков. Молодые ученые нашего института совместно с американскими коллегами проводят интереснейшие и обнадеживающие исследования с геном CD-подобного белка "вакцинных" штаммов вируса АЧС. Министерство образования и науки Российской Федерации в рамках МЦП ЕврАзЭС "Инновационные биотехнологии" финансирует выполняемые нами научно-исследовательские работы по созданию тест-системы для серодиагностики АЧС методом иммуноблоттинга на основе рекомбинантных иммунодоминантных белков. Полученные рекомбинантные конструкции будут полезны и в исследованиях по созданию кандидатных генно-инженерных вакцин.

Что такое стемпинг аут
Один из важнейших элементов современной политики контроля эпизоотических инфекций, буквально "подворный убой", stamping out-- в переводе с английского — ?тушить, затаптывать огонь, искоренять, подавлять, истреблять?. Процедура заключается в убое всех больных и подозреваемых в заражении (экспозированных) животных, утилизации, уничтожении их трупов (сжигании, захоронении), очистке и деконтаминации хозяйства. Ключевыми моментами процедуры стемпинг аут в современном понимании являются:
- обозначение зараженной территории;
- интенсивный надзор за болезнью с целью выявления зараженной территории и территории, где содержались опасно контактировавшие животные, или местности внутри этих зон;
- установление карантина и ограничение передвижения животных;
- немедленный убой всех восприимчивых животных, находящихся либо в зараженных и смежных помещениях, либо на всей зараженной территории; надежная утилизация туш животных и другого потенциально инфекционного материала;
- чистка и дезинфекция зараженных мест содержания животных;
- освобождение этих помещений от восприимчивых животных на необходимое время.
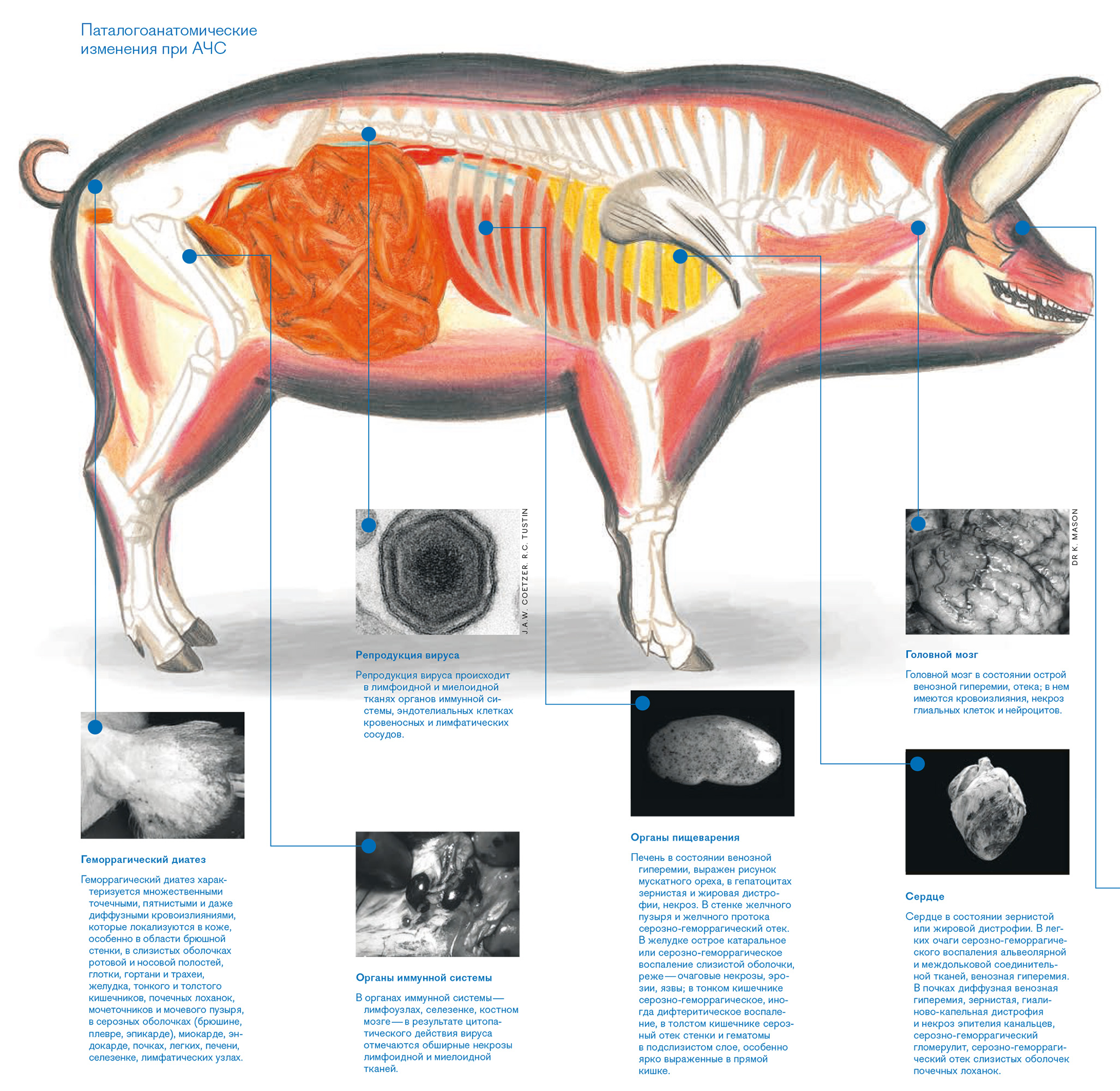
Вирус АЧС
Вирус АЧС классифицирован в отдельное семейство Asfarviridae. Крупные частицы вируса АЧС размером около 200 нанометров имеют сложное строение и округлую или икосаэдрическую форму.
В их архитектуре выявляются несколько слоев: внешняя оболочка, происходящая из клеточной мембраны и приобретаемая в процессе выхода из клетки почкованием, и внутренняя мембрана, окружающая икосаэдральный капсид, в центре которого расположена сердцевина из слоя фибриллярных компонентов и нуклеоида.
Вирус чрезвычайно устойчив к факторам различной природы, его выживаемость в объектах среды и продуктах свиного происхождения необычно высока. Вне организма в физиологических средах или сыворотке крови вирус сохраняется 6 лет при ?50°С, 18 месяцев в крови и сыворотке при комнатной температуре, до 1 месяца при +37°С. В полевых условиях он устойчив к гниению, длительно сохраняется в различных выделениях больных свиней: крови и тканях, истечениях, сгустках и т.п. Внутри организма больных свиней общая инфекционность туши превышает 1013 инфекционных единиц вируса; 96% ее аккумулируется в костном мозге.
Основной фактор непредсказуемого заноса АЧС в благополучные страны — сохраняемость вируса в пищевых продуктах.
Краткая история АЧС
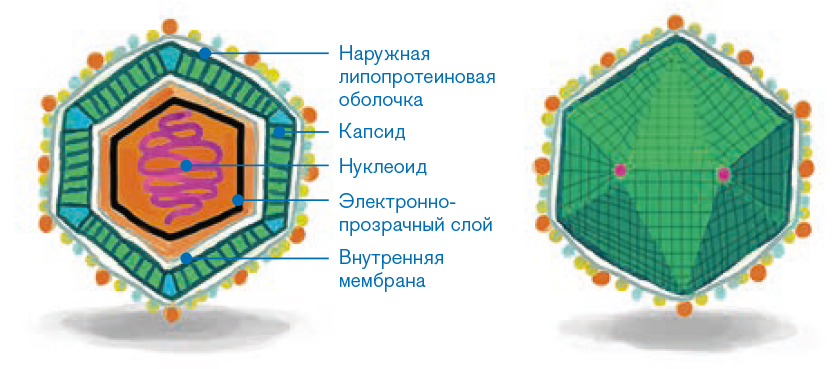
АЧС установлена более ста лет назад английским ученым Р. Монтгомери (R.E. Montgomery). Естественная история АЧС может быть разделена на четыре периода.
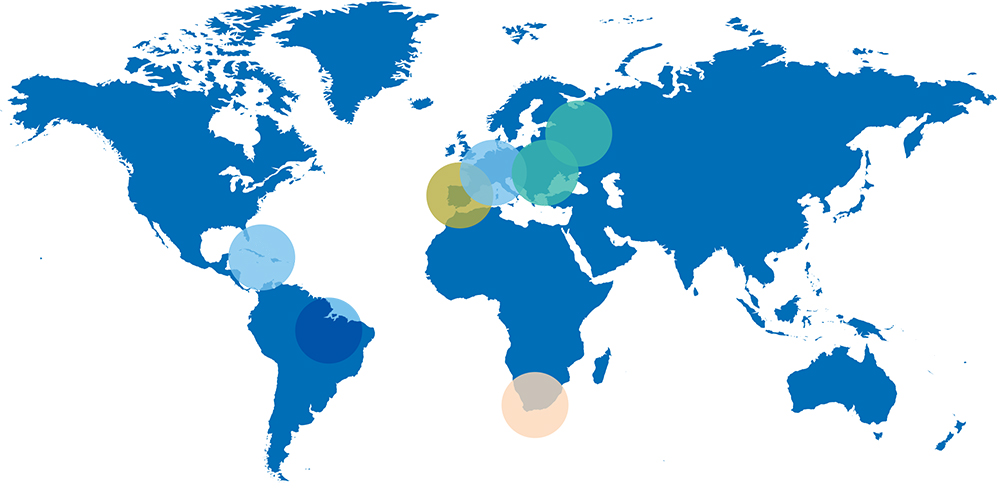
Распространение только в пределах традиционного южноафриканского нозоареала в природноочаговой форме с трансмиссивной передачей инфекции и редкими случаями острой летальной АЧС при заражении завезенных из Европы домашних свиней.
Возникновение, распространение среди домашних свиней и кабанов в Испании и Португалии, становление самостоятельного антропургического цикла и эндемии с рядом спорадических вспышек в других странах Южной Европы.
Эндемия в Испании и Португалии вплоть до ее успешного искоренения (1995), вспышки и эпизоотии АЧС в ряде стран Западной Европы, в СССР (1977), на Кубе (1971, 1980), на о. Гаити и в Бразилии (1978-1983).
Занос АЧС в Грузию, широкое распространение в юго-восточном регионе Евразии (Армения, Азербайджан, Абхазия, Нагорный Карабах, Россия, Иран, Украина, Латвия, Литва, Эстония, Белоруссия, Польша), становление эндемии на юге и в центре европейской части РФ.

