
Фото: Александр Кольцов
Заболевание периферических артерий (ЗПА) рис. 01 — одно из самых распространенных сосудистых заболеваний, оно наблюдается у более 10% людей старше 70 лет. Всего в мире от него страдают более 200 млн человек. У большинства заболевание не прогрессирует далее перемежающейся хромоты, но как минимум в 20% случаев его развитие приводит к хронической ишемии нижних конечностей (ХИНК). Ее симптомы — трофические язвы пальцев и стопы, боли в мышцах ног, сохраняющаяся перемежающая хромота и боли в икроножных мышцах при ходьбе — связаны с нарушением кровообращения в нижних конечностях из-за сужения или закупоривания (облитерации) артерий рис. 02. В каждом третьем случае состояние пациентов с ХИНК ухудшается, они получают диагноз КИНК (критическая ишемия нижних конечностей), при котором неизбежна ампутация. Летальность же после операций по ампутации достигает, по разным подсчетам, 20-25%.
рис. 01 Кровообращение в мыщцах у здоровых людей и у людей с патологией периферических артерий
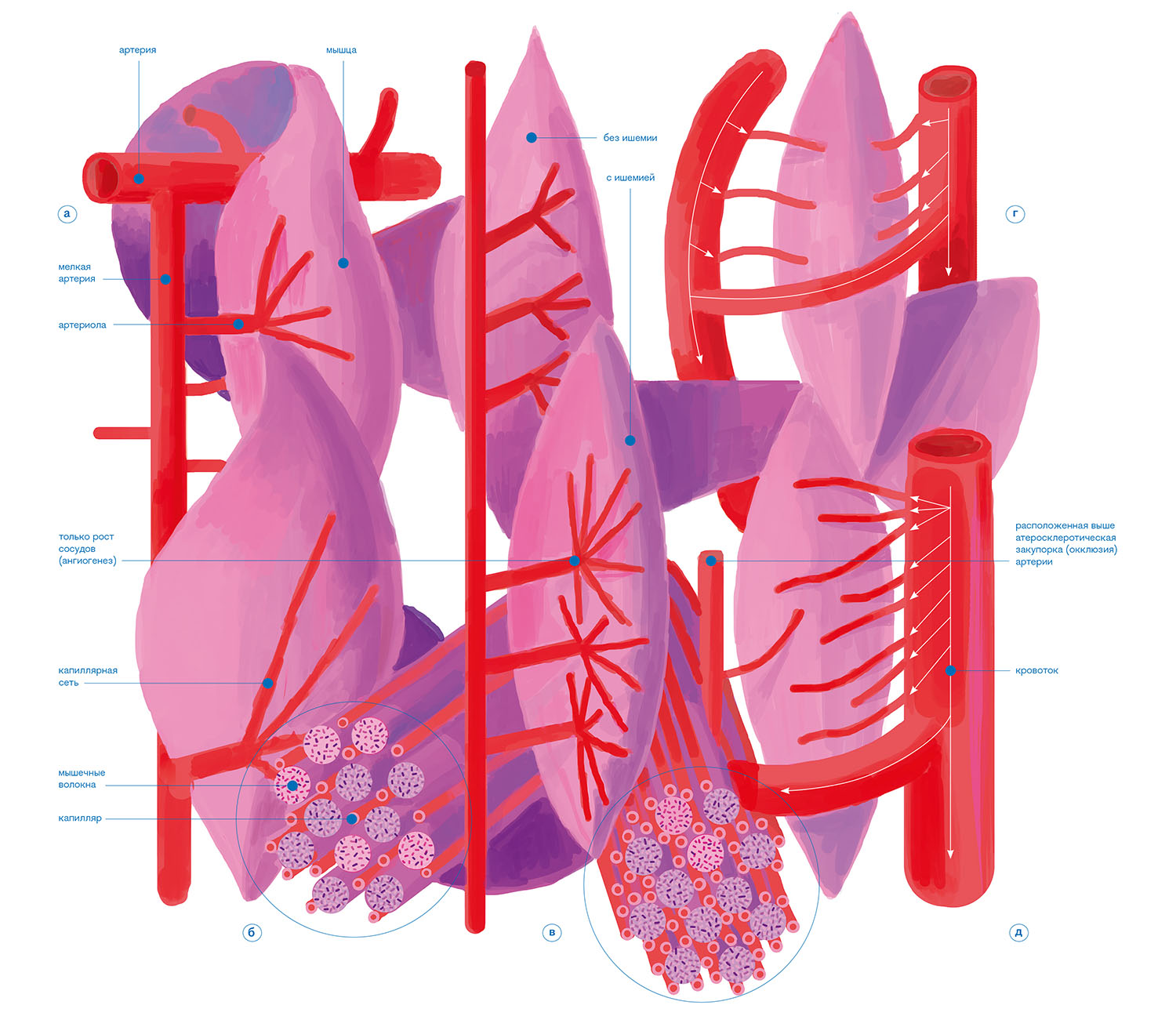
А) При отсутствии артериальных окклюзий кровоснабжение мышц ноги осуществляется через большие (>1мм) артерии, мелкие (от 200 мкм до 1мм) артерии, артериолы (от >20 мкм до <200 мкм) и капилляры (8-10 мкм). Капилляры не имеют гладкомышечной оболочки, но тем не менее могут регулировать кровоток.
Б) Детали (поперечный разрез) капиллярного кровообращения, которое доставляет кислород, обеспечивая метаболические потребности мышечных клеток скелетной мускулатуры, при отсутствии болезни.
В) При ишемии мышцы ангиогенез приводит к развитию дополнительных капиллярных ветвей каждой артериолы (также показано на поперечном срезе). Увеличение количества капилляров приводит к снижению сосудистого сопротивления и кровотока в артериолах.
Г) Две сообщающиеся между собой артериолы и их капиллярное ложе.
Д) Атеросклеротическая окклюзия останавливает кровоток в одной из артерий, и за счет ангиогенеза увеличивается размер сосуда между артериолами, увеличивается число и размер капилляров. Кровоток через увеличенные и дополнительные сосуды возрастает настолько, что может двигаться в обратном направлении.
рис.02 Проявления заболеваний периферических артерий в результате атеросклеротической окклюзии крупных артерий нижних конечностей
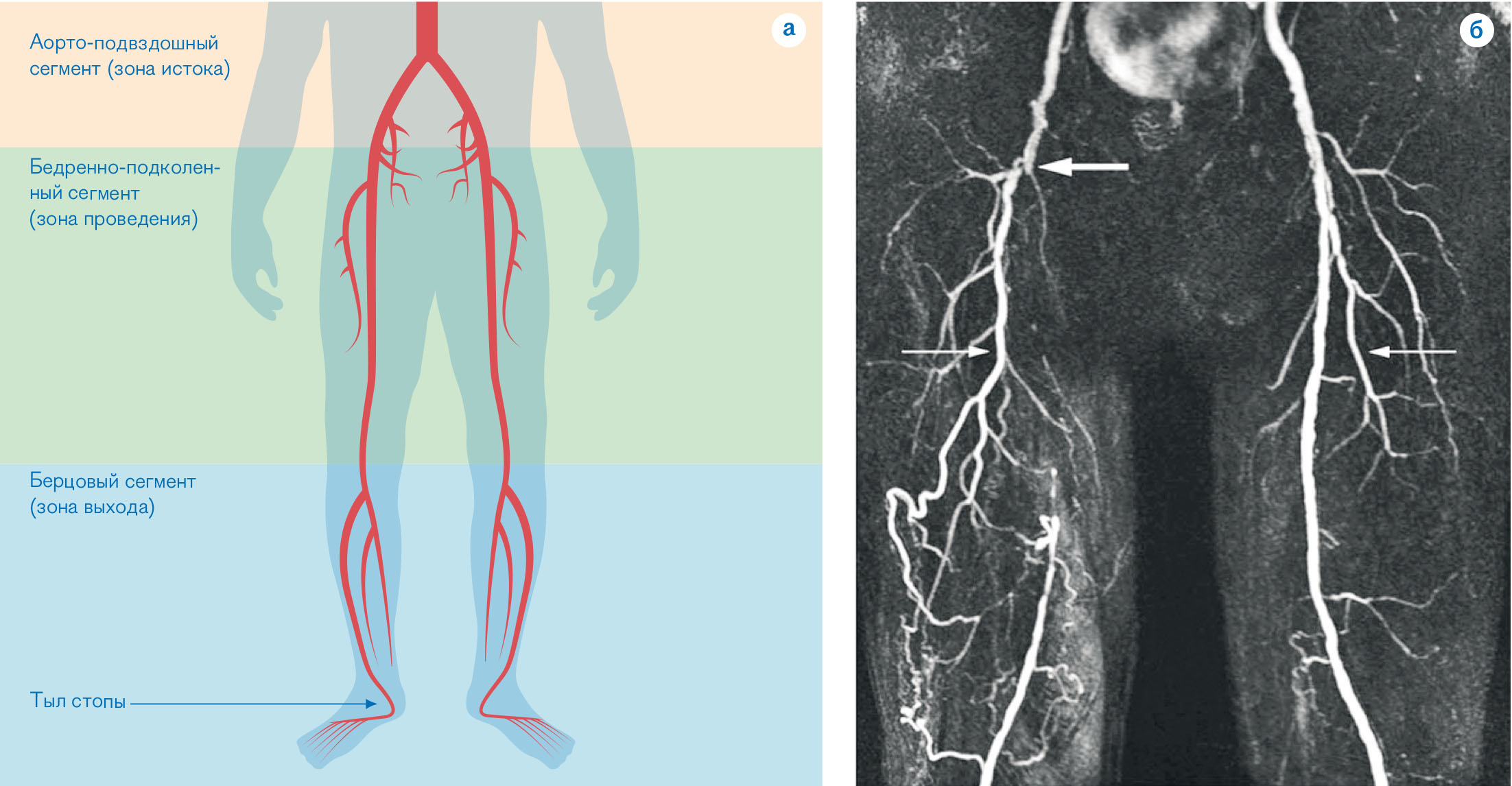
Кровоток от аорты к стопе проходит через общую и наружную подвздошные артерии (зона истока), бедренную и подколенную артерии (зона проведения) и через артерии, расположенные ниже колена. Когда на этом пути где-нибудь возникает окклюзия, кровоток начинает полностью зависеть от коллатеральных сосудов.
Б) Магнитно-резонансная ангиограмма показывает полную окклюзию бедренной артерии (толстая стрелка)
Б) Магнитно-резонансная ангиограмма показывает полную окклюзию бедренной артерии (толстая стрелка)
Один из основных способов борьбы с ХИНК — терапевтический ангиогенез, который подразумевает стимулирование образования новых сосудов. Ангиогенез — это естественный процесс при репарации тканей, но естественного его течения часто недостаточно для выздоровления.
Группа чебоксарских исследователей под руководством сосудистого хирурга Андрея Драгунова разработала метод стимуляции ангиогенеза в ишемизированных тканях через введение в зону поражения препарата на основе полипептидных факторов роста размерами 5-50 килодальтон (около 10 нм), полученного из собственной крови пациента, обогащенной тромбоцитами. Эта технология — усовершенствование метода улучшения коллатерального кровообращения, разработанного молдавским хирургом Петром Быткой. Еще в 1970-х годах, заметив, что на месте внутритканевой гематомы через некоторое время формируется соединительная ткань, богатая сосудами — мелкими капиллярами, артериолами и венулами (мельчайшими сосудами диаметром 15-100 мкм), Бытка предложил вводить в ишемизированные (то есть недостаточно кровоснабжаемые) ткани нижних конечностей собственную кровь пациента. В месте введения шел быстрый процесс неоваскуляризации — разрастания сосудов.
Неоваскулген
Как правило, для стимуляции ангиогенеза внутримышечно вводят в зону поражения ангиогенные факторы роста, а также клеточные материалы (клетки костного мозга; стволовые клетки, получаемые из различных тканей). Использование в терапии клеточного материала делает ее дорогостоящей. К тому же технологии с использованием клеточной терапии для стимуляции ангиогенеза до сих пор в России официально не разрешены. Единственное исключение — геннотерапевтический препарат неоваскулген, разработанный Институтом стволовых клеток человека (ИСКЧ) и хорошо зарекомендовавший себя в исследованиях: основной показатель для учета динамики ХОЗАНК (хронических облитерирующих заболеваний артерий нижних конечностей) — "дистанция безболевой ходьбы" — улучшился более чем на 110%. Осенью 2012 г. препарат поступил на российский рынок, текущая стоимость одного курса — 200 тыс. рублей. По словам Елены Романовой, пресс-секретаря ИСКЧ, сегодня 85-100% больных демонстрируют положительную динамику при лечении.
Андрей Драгунов еще в 2004 году предложил новый стимулятор ангиогенеза на основе клеток крови самого пациента (аутокрови). Увеличение количества коллатералей при ХИНК происходит не только за счет введения фактора роста эндотелия сосудов, но и других: фактора роста фибробластов, тромбоцитарного фактора роста, инсулиноподобного фактора роста, эпидермального фактора роста тромбоцитов. Метод предполагает, что все эти факторы роста поступают из аутокрови, которую забирают у пациента (400-600 мл, из локтевой вены). Кровь помещают в контейнер, установленный в сепаратор-центрифугу, разделяющий компоненты крови на фракции. Полученную таким образом эритромассу возвращают пациенту, а обогащенную тромбоцитами аутоплазму вводят в зоны ишемизированных тканей. "Поступающие с ней ангиогенные белки, — объясняет Драгунов, — действуют как синергисты. Этот эффект позволяет стабилизировать вновь образованные сосудистые структуры, что впоследствии приводит к формированию сложной "сети" из сосудов-коллатериев. То есть способ не только инициирует рост новых сосудов микроциркуляторного русла, но и позволяет сохранить плотность капиллярного русла в течение многих лет".

Ангиогенез в онкологии
С 2005 года Драгунов патентует постоянно обновляемый метод. Тогда же начались и клинические испытания на базе Республиканского кардиологического диспансера Минздравсоцразвития Чувашии. У 65% участников исследований наблюдался облитерирующий атеросклероз артерий нижних конечностей, у 32% — облитерирующий тромбангиит нижних конечностей, у 3% — постэмболическая окклюзия артерий нижних конечностей. Через полгода наблюдений дистанция безболевой ходьбы увеличилась на 325%. К тому же, если стандартно к четвертому году наблюдения пациентов после операции проходимость сосудистых протезов снижалась до 58,3%, то при терапевтическом ангиогенезе Драгунова — до 78,3%. Его компания "АнгиоЛаб" уже провела более 70 операций пациентов с ЗПА нижних конечностей. По результатам наблюдения всех этих случаев, частота тромбозов сосудистых протезов после реконструктивных операций в сочетании со стимуляцией ангиогенеза на горизонте 4 лет снижается почти на 20%. При этом курс лечения на основе аутокрови обходится в 10-40 тыс. рублей.
После 6 лет исследований Драгунов получил разрешение Росздравнадзора на использование технологии по всей России.
В ближайших планах "АнгиоЛаб" — открыть в Чебоксарах собственную клинику и обучающий центр для сосудистых хирургов, а также приступить к лицензированию терапевтического метода для других клиник в России и за рубежом. Для этого компании потребуется около $1-3 млн, и сейчас основатели проекта ищут российских инвесторов.
Драгунов планирует, что разработанная технология сможет применяться и для лечения ишемической болезни сердца (ИБС). Под новый проект "АнгиоЛаб" получил статус участника фонда "Сколково" и надеется привлечь грант фонда инноцентра.
Как сейчас лечат ХИНК
Внимание ученых к применению ангиогенеза в лечении именно ХИНК, по словам Драгунова, во многом связано с тем, что проблему адекватного восстановления кровообращения в нижних конечностях сложно решить с помощью сосудистых реконструкций — требуется хирургическое вмешательство. Сейчас в российских отделениях сосудистой хирургии при лечении ХИНК применяется эндартерэктомия (удаление атеросклеротических отложений из просвета артерии), стентирование (установка стента для расширения просвета сосуда), а также шунтирование (с помощью шунта — участка другого сосуда — создается обходной путь для крови) артерий и другие виды протезирования. Но в 10-15% случаев артерии нижних конечностей из-за выраженного их поражения вообще невозможно шунтировать. К тому же после таких операций остается проблема нарушения коллатерального кровотока — микроциркуляция крови, стимулирование которой крайне важно в патогенезе всех хронических облитерирующих заболеваний, не нормализуется в течение 2-3 лет после операции, а из-за продолжающегося прогрессирования основного патологического процесса может даже ухудшиться. Нарушение кровообращения на уровне микроциркуляции ведет к тромбозам сосудистых протезов, в результате необходимы повторные операции.

