Качество жизни больных рассеянным склерозом можно улучшить
Иммунология
Биофармацевтическая компания "Биокад" разработала инновационный препарат пэгилированного интерферона- бета-1а для лечения рассеянного склероза и провела его доклинические испытания. Проект получил поддержку ФЦП "Развитие фармацевтической и медицинской промышленности Российской Федерации на период до 2020 года и дальнейшую перспективу", мероприятие "Доклинические исследования инновационных лекарственных средств", контракт N16.N08.12.1015. Сейчас ведутся клинические испытания препарата.
Как лечить
Пятнадцать-двадцать лет назад появился новый класс препаратов, обнадеживший больных и врачей, — рекомбинантные бета-1а-интерфероны; они изменяют сам прогноз течения рассеянного склероза. В России зарегистрировано два препарата на основе бета-1-а-интерферона, оба иностранные: авонекс (США) и ребиф (Швейцария). К недостаткам обоих относится их короткое действие: авонекс нужно вводить раз в неделю, а ребиф — через день; а поскольку применять их надо очень долго, возникают побочные эффекты: местные, от частых инъекций, в виде инфильтратов и болезненности, и общие, характерные для применения инъекционных форм интерферонов, самый неприятный — гриппопободный синдром. Качество жизни больных, и без того невысокое, может ухудшиться, может пойти речь об отмене терапии интерфероном.

Что такое рассеянный склероз
Рассеянный склероз — далеко не первое заболевание, которое лечится интерферонами, достаточно вспомнить о гепатитах. Фармакологи умеют удлинять перерыв между инъекциями методом пэгилирования интерферонов — эта модификация заключается в химическом связывании молекулы белка с нетоксичным инертным полимером — полиэтиленгликолем (ПЭГ), мономер которого — этиленоксид. Присоединение ПЭГ не меняет структуры белка, но пэгилированная молекула имеет гораздо большую массу и больший гидродинамический радиус, чем непэгилированная; а значит, период полувыведения ее увеличивается, снижаются и колебания концентрации интерферона в крови. Присоединение ПЭГ к интерферону приводит, кроме того, к повышению стабильности, снижению иммуногенности и токсичности препарата. У пегилированных интерферонов снижена специфическая биологическая активность in vitro, но в организме (in vivo) активность пэгилированного препарата значительно выше — за счет длинного действия.
Как разрабатывался пэгилированный интерферон
Перед сотрудниками "Биокада" стояла задача обеспечить минимальную потерю активности пэгилированного препарата in vitro и достичь максимально пролонгированного действия in vivo.

Северная болезнь
Оптимизации подверглись следующие параметры пэгилирования: молекулярная масса ПЭГ; тип активированного ПЭГ; наконец, условия проведения реакции пэгилирования. Особенно важен был третий параметр: при разработке технологии нужно было связывать ПЭГ с теми сайтами молекулы интерферона, которые не участвуют во взаимодействии с клеточным рецептором. Как было установлено, наименее критичным для проявления активности молекулы бета-1а-интерферона in vitro является ее N-концевой участок (аминогруппа белка, с которой начинается его молекула) рис. 01.
рис. 01 Пэгилированный бета-1а-интерферон
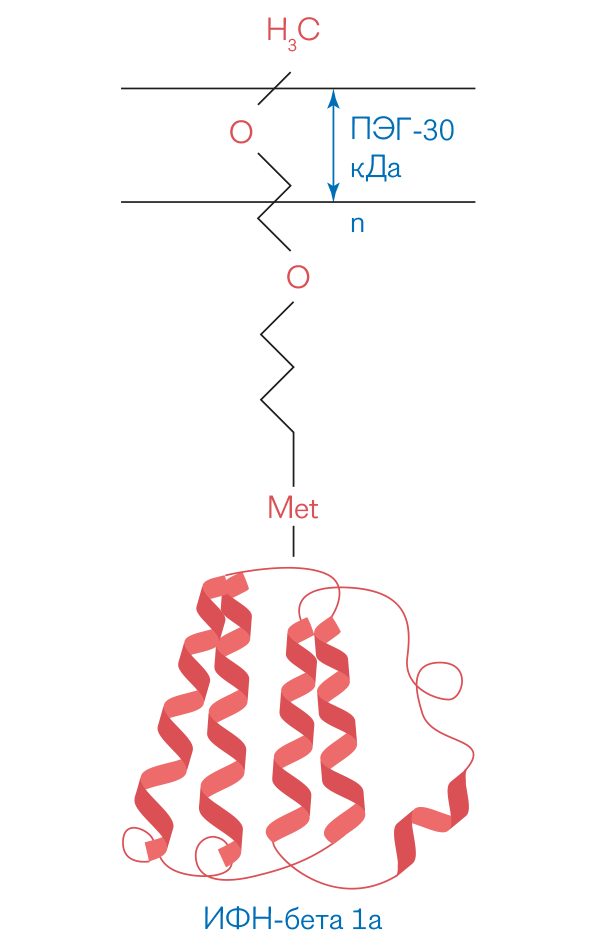
Молекулярная масса ПЭГ для модифицирования интерферона была выбрана в 30 тыс. дальтон — именно такой ПЭГ можно было присоединить строго в одном месте белка через альфа-амино-группу N-концевой аминокислоты.
В реакционной смеси по ходу реакции происходило образование более высокомолекулярного пэгилированного бета-1а-интерферона, а содержание нативного интерферона снижалось — со 100% до 20%. Очищенный пэгилированный интерферон выделяли из реакционной смеси методом ионнобменной хроматографии и исследовали его свойства. Пэгилированный бета-1а-интерферон оказался высокоочищенным и гомогенным продуктом с чистотой более 98%. Масс-спектрометрия показала, что пэгилированный бета-1а-интерферон — конъюгат, в котором одна молекула интерферона соединена с одной молекулой ПЭГ молекулярной массой 30 кДа через альфа--аминогруппу N-концевого метионина.
После мыши — человек
Доклинические исследования включают в себя исследование специфической активности in vitro и in vivo, фармакокинетики, общетоксического действия препарата и специфических видов токсичности. Исследование специфической токсичности направлено на выявление репродуктивной токсичности (эмбриотоксичности, тератогенности, влияния на генеративную функцию), арергенности, иммунотоксичности и мутагенности фармакологического средства.
Разработанный "Биокадом" пэгилированный бета-1а-интерферон — оригинальный препарат, так что сотрудники Отдела доклинических исследований и Лаборатории экспериментальной биологии "Биокада" провели максимально подробное исследование токсичности на трех видах животных (мышах, крысах и обезьянах) в сравнении с немодифицированным пэгилированным бета 1а-интерфероном (ребиф). Все исследования доказали, что пэгилированный препарат от "Биокада" потенциально безопасен для человека.
Слабей in vitro, сильней in vivo
В большинстве случаев ПЭГ-модификация приводит к снижению спе-цифической биологической активности in vitro — из-за экранирования сайтов белка. Исследователям "Биокада" необходимо было подтвердить, что их пэгилированный интерферон активность сохранил. Важнейший показатель биологической активности интерферонов при лечении рассеянного склероза — индукция синтеза белка МхА, определяющего резистентность человека и приматов к миксовирусам (этот белок индуцируется исключительно интерферонами 1-го типа). Исследователи "Биокада" обнаружили, что активность пэгилированного бета-1а-интерферона in vitro составляет примерно 47% активности немодифицированного интерферона. Соответственно, и среднеэффективная доза (ЕД50), вызывающая 50-процентную стимуляцию синтеза МхА в клетках, для пэгилированного интерферона была примерно в два раза выше, чем для немодифицированного.

Дать им стероиды
Специфическую активность пэгилированного бета-1а-интерферона in vivo исследовали по его способности индуцировать синтез неоптерина у макак резус. (Неоптерин — метаболит нуклеиновых оснований, предшественник биоптерина, который активирует лимфоцитоз, то есть иммунный ответ.) Выяснилось, что активность пэгилированного интерферона in vivo значительно выше, чем у немодифицированеного: подкожное введение и того, и другого запускало синтез неоптерина, но ответ на пэгилированный белок был на 200 часов длинней.
Опыты на мышах и обезьянах показали также, что пэгилированный бета-1а-интерферон характеризуется более низким клиренсом и более длительным периодом полувыведения из организма животных, чем обычный: 42 часа против 7 часов после введения 6 мкг на килограмм веса; полностью обычный интерферон после введения указанной дозы выводился за 24 часа, а пэгилированный — за 336 часов рис. 02. Это значит, что пэгилированный интерферон можно вводить больным рассеянным склерозом гораздо реже, чем авонекс или ребиф, а именно, раз в две-три недели.
рис. 02 Фармакокинетика интерферонов при однократном подкожном введении обезьянам