Фармагеддон не за горами
Новые импортные лекарства в 2016 году не будут допущены на российский рынок
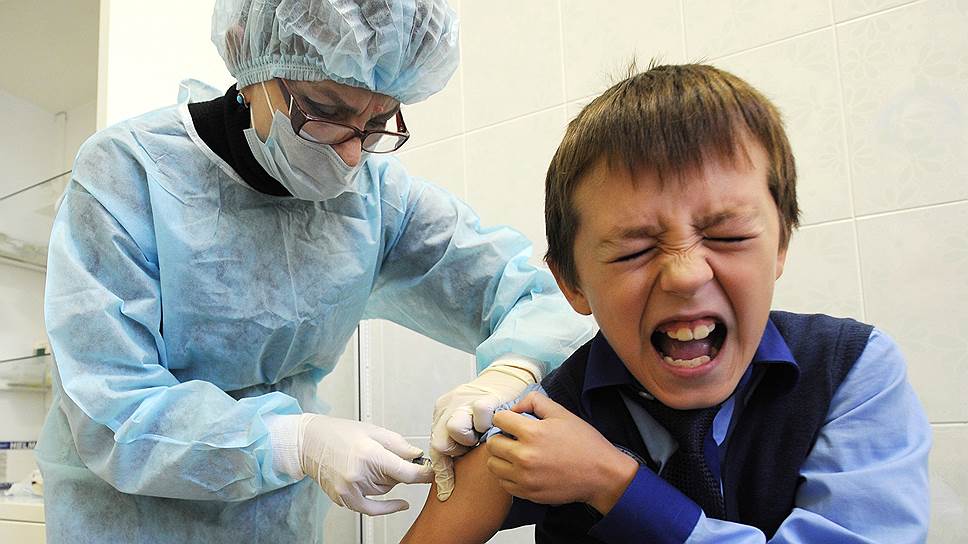
С 1 января 2016 года иностранные фармкомпании не могут зарегистрировать в России новые лекарственные препараты без подтверждения соответствия своих стандартов качества российским требованиям по стандарту GMP. Однако Минпромторг пока не наделил полномочиями проводить инспекции лекарственных заводов за границей ни одно из подведомственных учреждений. Если правительство в самое ближайшее время не отложит введение требования сертификатов, на российский рынок в этом году, по оценкам экспертов, не попадет ни один новый импортный лекарственный препарат. Проблемы возникли и у поставщиков в Россию иностранных вакцин.
Фото: РИА Новости
Введение новых требований к иностранным фармкомпаниям с начала 2016 года означает ограничение доступности современных лекарств для населения России, заявил "Ъ" Владимир Шипков, директор Ассоциации международных фармацевтических производителей (AIPM). По его словам, из-за изменений законодательства РФ с 1 января 2016 года иностранные производители не могут начать процесс регистрации в стране новых препаратов, не получив предварительно заключения о соответствии присвоенного им международного сертификата GMP (в российской версии — "Правила организации производства и контроля качества лекарственных средств") российским требованиям. Однако, как отмечает господин Шипков, для работы российского инспектората попросту отсутствует правовая база: получить сертификат негде и не у кого.
Напомним, появление новых требований к регистрации иностранных препаратов — часть процесса перехода всей российской фармотрасли на стандарты GMP, которые используют мировые производители лекарств. Интересно, что уже и раньше в этом процессе происходили существенные смещения установленных сроков начала действия того или иного документа. Например, согласно тексту принятого еще в 2010 году федерального закона "Об обращении лекарственных средств", все российские производители должны были получить российскую версию сертификатов до 31 декабря 2013 года. Однако за это время так и не были подготовлены документы, регламентирующие условия и процедуру подтверждения производства этим стандартам: "Правила..." прошли все процедуры согласования и вступили в силу только в ноябре 2013 года. Пройти сертификацию за два месяца было бы невозможно как из-за неготовности сертификационных органов, так и из-за числа потенциальных клиентов: инспекторату пришлось бы проверить около 500 площадок российских производителей. Впоследствии правительство выпустило постановление, которое установило для компаний новый срок — до 2016 года. При этом с 2016 года также стало обязательным наличие именно российской версии GMP для тех иностранных производителей, которые собираются выводить на российский рынок новые препараты, а с 2017 года — для всех иностранных фармкомпаний.
"Правила организации и проведения инспектирования производителей, а также выдачи заключений о соответствии производителя лекарственных средств указанным требованиям были утверждены правительством лишь 3 декабря 2015 года, 18 декабря вступили в силу",— отмечает господин Шипков. Из-за этого нормативно-правовые акты, необходимые для определения порядка выдачи заключений о соответствии, формы заявления на проведение инспекции, инспекционного отчета, заключения о соответствии, а также методики расчета платы за инспектирование производственных площадок, расположенных за пределами РФ, не готовы. В результате на данный момент учреждения, которое могло бы осуществлять прием заявлений от производителей и заключать договоры на проведение инспекции их площадок, просто не существует. "Одновременно много вопросов возникает к качественному и количественному составу инспектората, способного на высоком профессиональном уровне обеспечить исполнение государственной функции",— добавляет господин Шипков. Таким образом, по его словам, стандарт GMP превратился в дополнительный и сейчас непреодолимый административный барьер для цивилизованных международных производителей и используется как средство антиконкурентной борьбы, создающее преимущества для отечественных компаний.
Объем российского фармрынка составлял в 2015 году около 1 трлн руб., около 65% его приходится на импорт. Оценить долю препаратов, которые за счет сложившейся ситуации не появятся на рынке, сейчас невозможно, но оценки в единицы миллиардов рублей неосуществленных продаж не выглядят завышенными — причем речь идет именно о препаратах и лекарственных формах, дающих больший эффект при терапии.
Минпромторг на запрос "Ъ" в связи с заявлением главы AIPM не ответил.
Практика проверки иностранных сертификатов GMP инспекцией на локальном рынке в целом существует на международном уровне. Однако в большинстве случаев с такой процедурой сталкиваются фармкомпании из развивающихся стран. В Европе взаимное признание сертификатов GMP происходит между странами, ратифицировавшими конвенцию о сотрудничестве фармацевтических инспекций (PIC). "Оптимальным вариантом для России было бы присоединиться к этому объединению, так как это позволило бы определять необходимость проверки сертификата иностранной компании по национальному признаку и, соответственно, не инспектировать предприятия известных европейских производителей с мировой репутацией",— говорит глава DSM Group Сергей Шуляк. Сейчас же, по его словам, пока неустановленной российской службе предстоит за год проверить около 400 иностранных фармкомпаний, которые сейчас работают на российском рынке.
"Учитывая опыт инспектирования российских предприятий за прошедшие несколько лет, в среднем сертификацию проходят не более ста компаний в год. Сократить сроки проверки невозможно по технологическим причинам, а чтобы существенно увеличить число проверяющих, потребуется около года из-за срока обучения новых инспекторов GMP",— отмечает господин Шуляк. Из-за отсутствия процедуры проверки уже в 2016 году на российский рынок могут не попасть около 50 инновационных продуктов и еще столько же дженериков и препаратов, отличающихся от существующих лекарственной формой.
Основная причина задержки оформления всех необходимых для создания института инспектората документов, по мнению Давида Мелик-Гусейнова, директора ГБУ НИИ организации здравоохранения,— "бюрократические проволочки ведомств". "Аналогичная ситуация складывается и с выдачей сертификатов GMP российским предприятиям — большая часть из них, несмотря на окончание в прошлом году переходного периода, так и не получили документы",— говорит господин Шуляк. Отметим, что несоответствие нормативных требований и существующих у ведомств ресурсов с этого года также стало препятствием для регистрации в России и новых партий иностранных вакцин.
Скорее всего, так или иначе в ближайшее время правительству придется переносить сроки переходного периода для иностранных препаратов. Тем более что такая практика в процессе перехода российской фармотрасли на GMP уже есть, отмечает господин Мелик-Гусейнов.