Расчет на растворение
В мире постоянно проводятся исследования новых лекарств — сначала в лабораториях, а потом на добровольцах. Российские ученые предложили новую методику оценки препаратов, которая позволит избежать тестирования лекарств на людях.
Справка
In vitro (лат.— "в стекле") — это технология выполнения экспериментов, когда опыты проводятся "в пробирке" — вне живого организма. Многие эксперименты, имеющие отношение к молекулярной биологии, биохимии, фармакологии, медицине, генетике и др., проводятся вне организма — на культуре живых клеток или в бесклеточной модели. Эксперименты in vitro в тех случаях, когда альтернативой являются исследования на животных или человеке, считаются менее достоверными и часто бывают лишь необходимой предварительной стадией для оценки возможности и необходимости последующих исследований. Однако они часто удешевляют предварительные стадии исследования и позволяют сохранить жизнь подопытных животных.
In vivo (лат. — "в (на) живом"), то есть "внутри живого организма" или "внутри клетки". В науке in vivo обозначает проведение экспериментов на (или внутри) живой ткани при живом организме. Такое использование термина исключает использование части живого организма (так, как это делается при тестах in vitro) или использование мертвого организма. Тестирование на животных и клинические испытания являются формами исследования in vivo.
Ex vivo (лат.— "из жизни") — технология экспериментов в живой ткани, перенесенной из организма в искусственную внешнюю среду. Наиболее распространенная техника ex vivo использует живые клетки или ткани, извлеченные из живого организма и выращенные (сохраненные) в стерильных лабораторных условиях в течение нескольких дней или недель. Такие клетки служат образцами поведения организма в целом, как следствие, сокращается потребность в экспериментах над животными и человеком.
Клинические испытания препарата — научное исследование эффективности, безопасности и переносимости лекарства. В здравоохранении клинические испытания проводятся для того, чтобы собрать данные о безопасности и эффективности новых лекарственных препаратов или устройств. Такие испытания проводятся только после того, как собрана удовлетворяющая информация о качестве продукта, о его доклинической безопасности, а также получено разрешение на проведение клинического испытания от уполномоченной организации.
Тестирование должны проходить все препараты, даже так называемые дженерики — копии оригинального препарата. Оригинальный препарат — это новое, впервые синтезированное и прошедшее полный цикл исследований лекарственное средство. Его активные ингредиенты защищены патентом на определенный срок, а на разработку, клинические испытания, производство и выпуск препарата на рынок затрачены значительные интеллектуальные и материальные ресурсы. В большинстве развитых стран для охраны приоритета разработчика оригинального препарата монопольное право патентообладателя ограничено сроком действия патента (в РФ — 20 лет) и территорией страны, в которой он действует. По окончании срока действия патента любая фармацевтическая компания может приобрести право производить копию оригинального препарата — дженерик.
Дженерик — это лекарственный препарат с доказанной фармацевтической, биологической и терапевтической эквивалентностью с оригиналом. То есть лекарственное средство, имеющее такой же состав действующих веществ, лекарственную форму и эффективность, как и оригинальный препарат, но не обладающее патентной защитой. Цена на дженерики обычно значительно ниже, чем на оригинальные препараты, при этом дженерики не отличаются от оригинальных средств по эффективности и безопасности и производятся в строгом соответствии с установленными регламентами и стандартами качества. Использование дженериков имеет большое медико-социальное значение, поскольку делает качественное лечение доступным для широких слоев населения.

Однако помимо действующего вещества (в дженерике и оригинальном препарате оно одинаковое) в состав препарата входят и вспомогательные: наполнители, целлюлоза, лактоза и другие. У каждого производителя они свои, и они могут влиять на эффективность препарата.
Существует двухступенчатая система исследования дженериков. Сначала их тестируют в пробирке, то есть in vitro, а потом, если результаты первых тестов положительные, переходят к исследованиям на здоровых добровольцах — in vivo. По результатам таких испытаний оценивают, как препарат растворяется и всасывается организмом человека.
Добровольцы принимают лекарство, а затем через определенные промежутки времени у них берут кровь на анализ. Из проб крови выделяют плазму, а из нее — действующее вещество препарата. Концентрация препарата в крови в тот или иной момент определяется с помощью хроматографа. На основе полученных данных в лаборатории стоят фармакокинетическую кривую и сравнивают ее с кривой, полученной при испытании оригинального препарата. Если кривые совпали, лаборатория выдает заключение, что дженерик можно выпускать в производство.
Однако испытания на людях даже в стадии клинических исследований всегда риск для их здоровья. Кроме того, испытания на группе добровольцев требуют от фармацевтической компании немалых ресурсов, что повышает стоимость лекарств, которые она выпускает.
Игорь Шохин, доктор фармацевтических наук, выпускник Московской медицинской академии им. И. М. Сеченова (сейчас Сеченовский университет) и руководитель Центра фармацевтической аналитики, разработал методологию, которая позволяет перенести второй этап исследований нового препарата в лабораторию. Сотрудники центра с помощью специального аппарата могут моделировать условия, в которых препарат оказывается, попав в желудок. Можно менять кислотность и температуру, имитируя прием лекарства натощак, когда кислотность выше обычной, или на полный желудок, когда кислотность понижается, а температура может повыситься. В обоих случаях важной частью процесса является перемешивание раствора с определенной частотой.
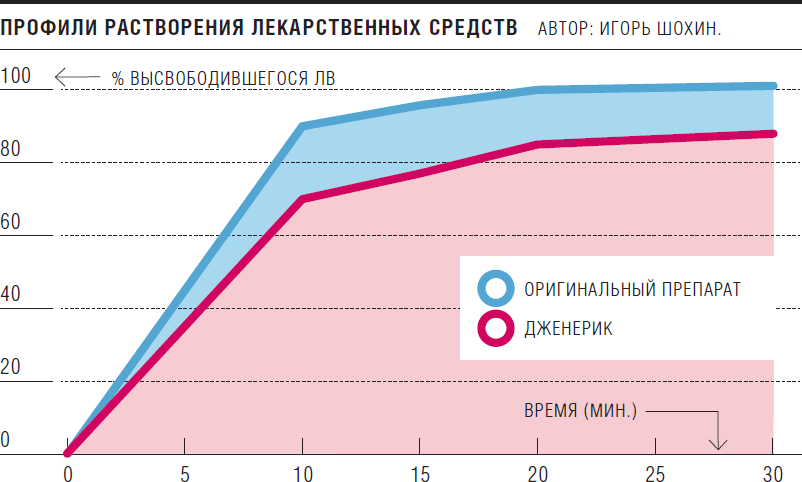
Через какое-то время после растворения таблетки необходимо взять пробы жидкости и проанализировать их на спектрофотометре. Прибор позволяет оценить, в какой момент оболочка таблетки начала растворяться, а активные вещества — высвобождаться. По результатам анализа исследователи строят кинетическую кривую растворения, которую оценивают с помощью математического анализа, и устанавливают, насколько кривая растворения нового препарата отличается от аналогичных данных для оригинального.
Игорь Шохин: меньше людей подвергнет опасности свое здоровье, пусть даже и добровольно
BUSINESS GUIDE: Как вам удалось создать методологию оценки профилей растворения препарата?


