Сохраняя текучесть крови
открытие
По заболеваниям сосудов головного мозга Россия занимает первое место в мире. Статистика утверждает, что ежегодно в России фиксируется около 450 тыс. случаев инсультов. При этом более 200 тыс. человек умирают, около 160 тыс.— становятся инвалидами. Лишь три года назад на рынке появился препарат (на основе действующего вещества дабигатран), который практически сразу же после выхода на рынок стал золотым стандартом при борьбе с инсультом.

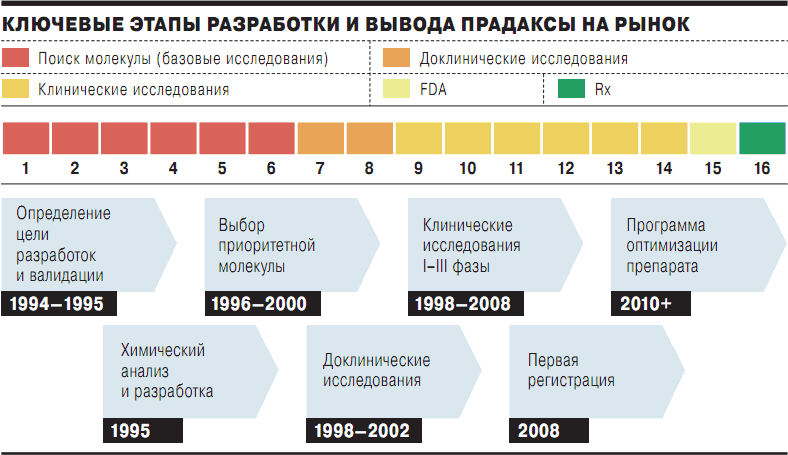
Более 16 лет прошло от начала работ по выявлению молекулы до выхода прадаксы на рынок борьбы с инсулином
Фото: Boehringer Ingelheim
Мерцательный риск
Важность крови как элемента организма ясна для человека с глубокой древности. Кровопускание как лечебная процедура применялось врачами Древней Греции, Рима. Изображение пациента, которому пускают кровь из ноги и шеи, сохранилось на одной из фресок в египетской пирамиде, датированной серединой третьего тысячелетия до н. э. Считалось, что здоровье человека обусловлено балансом крови и других физиологических жидкостей. Сердце же, по предположению Аристотеля, является центральным органом всего человеческого организма.
В теле человека более 100 тыс. км сосудов и около 5-6 л крови. В сохранении здоровья, и даже жизни, очень важную роль играет свертываемость крови, или коагуляция,— это основное средство, которым организм залечивает раны. Главным действующим элементом этого процесса является фибриноген. Например, когда происходит повреждение сосуда, в крови запускается так называемый коагулирующий каскад — цепная реакция, в которой принимают участие молекулы, иногда называемые факторами. Этот процесс приводит к связыванию кровяных бляшек с поврежденной тканью. Затем активируется фактор коагуляции под названием тромбин, и растворимый в крови фибриноген начинает формирование в сосуде устойчивой сетки. Кровяные клетки улавливаются этой сеткой, и таким образом формируется сгусток крови, тромб. Именно этот сгусток крови залечивает повреждение сосудов и предотвращает потерю крови. То есть способность крови к свертыванию буквально спасает жизнь. Однако это свойство надо контролировать, поскольку при определенных условиях свертываемость крови нарушается. Самое известное нарушение свертываемости крови известно как гемофилия. Это наследственное заболевание, при котором одного из факторов коагуляционного каскада нет в достатке, поэтому сгусток крови не формируется и кровотечение может продолжаться гораздо дольше, чем в здоровом организме.
Но есть и другое нарушение, встречающееся гораздо чаще,— когда риск образования тромбов повышается, а не понижается. В этом случае тромб может стать причиной инсульта. В частности, риску инсульта подвержены люди с мерцательной аритмией или фибрилляцией предсердий (ФП) — нарушением сердечного ритма. Это наиболее часто встречающееся нарушение сердечного ритма — примерно у каждого четвертого человека в возрасте после 40 лет. При аритмии возрастает риск образования тромбов в застойных зонах в сердце, которые могут оторваться, попасть в сосуд головного мозга и там привести к разрыву сосудов, то есть инсульту.
Инсульты на фоне ФП протекают более тяжело, с увеличением риска смерти (20%), а в 60% случаев человеку грозит инвалидность.
Конечно, больных, имеющих высокий риск инсульта, лечили и раньше, и нельзя сказать, что безуспешно. Им назначалась долговременная антикоагуляционная терапия при помощи так называемых антагонистов витамина К. К таким препаратам относится, например, варфарин, который был одобрен для лечения в начале 1950-х годов. Лечение этим препаратом проходило достаточно успешно: вероятность инсульта снижалась более чем на 60%. Но принимать этот препарат могли не больше половины тех, кому он предназначался, из-за ряда отягчающих факторов.
Во-первых, из-за достаточно узкого диапазона доз, при которых достигался необходимый эффект, то есть оптимальное свертывание крови: большая доза препарата могла привести к кровотечению, в то время как при малых дозах он не выполнял свою функцию. Во-вторых, из-за большой инерционности: препарат медленно начинал действовать и так же постепенно переставал, поэтому было довольно трудно предсказать реакцию организма на ту или иную дозу. В-третьих, варфарин вступал во взаимодействие со многими пищевыми продуктами и медицинскими препаратами, что могло изменить его терапевтический эффект либо в сторону кровотечения, либо в сторону образования тромба. Все это означало, что каждому пациенту необходимо было подбирать индивидуальную дозу, постоянно контролировать кровь, то есть часто сдавать ее на анализ.
Кстати, мерцательная аритмия не единственное заболевание, несущее опасность образования тромбов. Еще одним таким заболеванием является венозная тромбоэмболия, когда сгусток крови формируется в вене. Это не менее серьезно, чем нарушение сердечного ритма. Венозная тромбоэмболия стоит в списке сосудистых заболеваний с возможным летальным исходом на третьем месте после инфаркта и инсульта. Может показаться удивительным, но от венозной тробоэмболии умирает каждый год больше жителей Европы, чем от рака груди, простаты, ВИЧ и ДТП вместе взятых. Коварство этого заболевания заключается в чрезвычайной стремительности, что в итоге может привести к смерти.
Охота за молекулой
Необходимость найти удобный и эффективный препарат для борьбы с инсультами в случае мерцательной аритмии, а также лечения пациентов с диагнозом "венозная тромбоэмболия" стояла достаточно остро. Ученым предстояло разработать принципиально новый коагулянт. За решение этой задачи взялись ученые самой крупной в мире частной фармацевтической компании "Берингер Ингельхайм". Они понимали, что свои усилия должны сосредоточить на основном ферменте, участвующем в процессе коагуляции. Решением, по их мнению, должна была стать новая молекула, которая могла бы напрямую блокировать активную часть этого фермента — тромбина — и таким образом предотвращать чрезмерное образование сгустков крови. Свою цель — какими свойствами должен обладать новый коагулянт — они представляли достаточно четко.
"Мы хотели получить вещество, которое обладало бы мощным действием, долгосрочным эффектом, которое можно было бы принимать перорально, которое хорошо переносилось бы пациентом и не взаимодействовало с пищевыми продуктами",— говорит химик руководитель исследовательской команды компании "Берингер Ингельхайм" доктор Норберт Хауэль. В 1992 году появилась публикация, в которой убедительно излагалось, каким образом ингибитор (вещество, подавляющее действие) тромбина должен связываться с его активным участком. "Для нас эта публикация оказалась очень важна: мы увидели, что это возможно,— поясняет доктор Хауэль.— Молекула, подавляющая активность тромбина, должна подходить к молекуле тромбина, как ключ подходит к замку. Наши исследователи уже видели, какой должна быть формула молекулы ингибитора тромбина, чтобы она плотно прилегала к активному участку подавляемой молекулы". То есть исследователи с самого начала понимали, какую структуру надо синтезировать. При этом вся команда знала, что исследовательские команды других компаний тоже начали искать ингибитор тромбина с соответствующими свойствами. Вопрос был в том, кто первый найдет молекулу, которая впоследствии будет спасать миллионы человеческих жизней. В том же 1992 году ученые компании "Берингер Ингельхайм" стали искать эту молекулу.
Но знания того, что ищешь, недостаточно для подобных исследований. Ученые в команде доктора Хауэля представляли себе, какие физические силы действуют между отдельными атомами в молекуле тромбина, какие идут реакции и какая структура должна быть у требуемой молекулы. И создание молекулы поначалу продвигалось динамично: активность молекулы росла, формула приближалась к требуемой. Но в какой-то момент движение застопорилось, активность молекулы остановилась на уровне, далеком от требуемого. Поиски продолжались, но отчаяние росло. "Мы дошли до точки и дальше не могли повышать активность молекулы. Мы готовы были уже бросить эту работу,— рассказывал господин Хауэль.— А потом я понял, что добавление одной липофильной группы так искривляло форму молекулы, что она не могла приблизиться к активному участку молекулы тромбина. Для получения нужной формы требовалось очень много энергии".
Поняв причину неудач, исследовательская команда нашла выход — закольцевать структуру синтезируемой молекулы, сделать ее замкнутой. Это сработало. В результате появилась молекула, которой присвоили порядковый номер 1235. На данном этапе синтезированная молекула подходила к молекуле тромбина, как ключик к замку. Но это было только начало пути. Работа по оптимизации действия полученной молекулы, подгонке ее под самые строгие требования только начиналась.
Проанализировав нескольких сотен молекул, ученые остановили выбор на одной — под рабочим названием "бибр-590". После ряда опытов оказалось, что в пробирке (инвитро) эта молекула более или менее делает то, чего от нее ожидают, однако в крови (инвиво) такого эффекта почему-то нет. Эффекта не было даже при внутривенном введении вещества животному. После множества опытов эту молекулу решено было сделать более гидрофильной, чтобы белки крови не удерживали ее так крепко. И через восемь месяцев, попробовав еще около 50 вариантов рабочей молекулы, группа доктора Хауэля нашла соединение, которое подавляло активность тромбина не только инвитро, но и инвиво. Усовершенствованной молекуле дали название "бибр-642".
Порошок преткновения
Но впереди был еще не один этап создания лекарственного препарата. Следующим шагом исследователей стало повышение активности молекулы, чтобы она работала при более низких концентрациях. По словам Норберта Хауэля, здесь было найдено очень "элегантное решение": молекулу удлинили, и теперь она могла связывать несколько участков молекулы тромбина. Испытания продолжались. Было опробовано еще более 120 структур молекулы, прежде чем одна из них показала результаты, удовлетворившие ученых. Тесты инвитро и инвиво проходили ровно и демонстрировали стабильный эффект. Эта молекула с рабочим номером 953 уже удостоилась от исследователей отдельного названия — дабигатран.
Тесты становились все более сложными. В лабораторных условиях был разработан метод, помогающий моделировать условия тромбоза в человеческом организме. Новое вещество связывалось с молекулой тромбина быстро и обратимо, что также было очень важным условием. По сравнению с другими препаратами дабигатран показывал лучший эффект при более низких дозах.
Тесты препарата на мышах, кроликах, а затем и на приматах показали очень хорошие результаты: хороший коагулирующий эффект длился около восьми часов. Активность дабигатрана оказалась высокой как при венозном тромбозе, так и при артериальном.
К концу 1996 года у команды исследователей было достаточно результатов проведенных экспериментов, чтобы убедить руководство продолжать разработку и финансировать дальнейшую работу. Вещество обладало всеми необходимыми для лекарства свойствами: очень хорошей переносимостью, активностью после приема внутрь, достаточно длительным действием, стабильностью. И руководство приняло непростое решение — продолжать работу и инвестировать в разработку препарата миллионы евро. Непростым решение было потому, что успешным результат можно назвать только после клинических испытаний. А работы оставалось еще немало: разработать технологический процесс для производства вещества в достаточных количествах, найти оптимальную форму выпуска лекарственного препарата и провести масштабные испытания на людях. Пока у исследователей было всего 430 кг дабигатрана, который произвели в период с 1998 по 2001 год. Для испытаний его было достаточно.
Кислотная доза
С виду дабигатран был таким же, как 90% других веществ в фармацевтике,— белый порошок. Теперь ученым надо было придумать такую форму лекарства, чтобы этот порошок доставлялся в желудок и выполнял свои функции. Однако для того, чтобы препарат хорошо растворялся, нужна кислая среда. В менее кислой среде он растворялся хуже. А большинство пожилых людей имеют как раз пониженную кислотность, кроме того, многие принимают средства против изжоги. В итоге по результатам многих тестов оказывалось, что препарата в крови как будто и не было, то есть эффект от его приема был нулевой. Вокруг дабигатрана требовалось создать кислотный кокон, который сохранял бы необходимую кислотность до того, как вещество попадет в кровоток.
Найденное решение было связано с историческими корнями "Берингер Ингельхайм", поскольку начинала компания около 130 лет назад с производства винной кислоты, продукта виноделия, в регионе, где издавна выращивался виноград. Именно винная кислота обеспечивала дабигатрану наилучшую растворимость. Но если добавить этот компонент непосредственно к дабигатрану, он начнет распадаться еще до того, как попадет в желудок. Кислая среда должна была начинать действовать только после того, как препарат окажется внутри организма. Решение было найдено: на препарат наносили ультратонкий изолирующий слой растворимого в воде полимера, а сверху — слой винной кислоты. Когда пациент глотал таблетку, ультратонкий слой растворялся и основное вещество — дабигатран,— начинало взаимодействовать с кислотой. Этим обеспечивалась хорошая всасываемость лекарства даже при низкой кислотности желудочного сока.
Последний штрих к созданию лекарственного препарата — подбор торгового названия. Название лекарству, в котором действующим веществом является дабигатран, подбиралось несколько лет. Одному из международных агентств была поставлена задача создать такое название, которое врачи запоминали бы легко, а пациенты не путали с другими, которое звучало бы необычно и было узнаваемым на многих языках. Из сотен вариантов было выбрано необычное звучное слово — прадакса.
Появление прадаксы считается крупнейшим достижением за более чем полувековой период деятельности по созданию антикоагулянтов. Сегодня препарат одобрен и применяется во всем мире для профилактики инсульта при фибрилляции предсердий и системной эмболии у взрослых с несколькими факторами риска. По тем же показаниям в конце 2011 года препарат был одобрен к применению в России.

